
کلرید باریم نمک غیر آلی است که از کاتیونهای باریم (Ba +) و آنیونهای کلرید (Cl–) تشکیل شده است. این ماده جامد سفید رنگی است که محلول در آب و، رطوبت ساز است. فرمول شیمیایی کلرید باریم BaCl2 است. کلرید باریم در مقیاس صنعتی، از طریق یک فرآیند دو مرحله ای آماده می شود. از نمک های باریم در صنعت به وفور استفاده می شود. کلرید باریم از نظر ماهیت سمی است. کلرید باریم به عنوان یک نمک محلول و ارزان از باریم، در آزمایشگاه کاربرد گسترده ای پیدا می کند. در صنعت، کلرید باریم به طور عمده در تصفیه محلول نمک در گیاهان و همچنین در ساخت نمک های عملیات حرارتی، سخت شدن فولاد، در ساخت رنگدانه ها و ساخت سایر نمک های باریم استفاده می شود.
کلرید باریم
کلرید باریم | خرید کلرید باریم | فروش کلرید باریم | قیمت کلرید باریم | خرید | فروش

این ماده یک ترکیب غیر آلی با فرمول BaCl۲ است. به آن Barium Muriate یا Barium dichloride نیز گفته می شود. مولکول های این ماده دارای پیوند یونی بین کاتیون های باریم و آنیون های کلرید هستند. باریم فلزی است که در این نمک یونی حالت اکسیداسیون ۲+ نشان می دهد در حالی که کلر غیر فلزی است و حالت اکسیداسیون -۱ در BaCl۲ را نشان می دهد.
این ماده یکی از رایج ترین نمک های محلول در آب باریم است. مانند اکثر نمکهای باریم، سفید، سمی است و رنگ سبز و زرد به شعله می دهد. این ماده همچنین دارای رطوبت است و ابتدا به دی هیدرات BaCl۲ (H۲O) ۲ تبدیل می شود. کاربرد این ماده در آزمایشگاه و صنعت محدود است.
این ماده به دو شکل متشکل می شود. یک فرم دارای ساختار فلوریت مکعب (CaF۲) و دیگری دارای ساختار کوتونیت orthorhombic (PbCl۲) است. کووردیناسیون باریم در ساختار فلوریت ۸ و در ساختار کوتونیت ۹ است.این ماده در دمای اتاق کریستال منوکلینیک سفید براق، بدون بو، تلخ و شور است. این ماده محلول در آب، استون و در اتانول و اتر، اسید نامحلول است.
در محلول آبی این ماده مانند یک نمک ساده رفتار می کند. در آب به صورت یک الکترولیت ۱: ۲ است و محلول دارای PH خنثی است. محلول های آن با یون سولفات واکنش می دهند و رسوبی سفید و ضخیم سولفات باریم تولید می کنند.
Ba۲ + + SO۴۲− → BaSO۴
با اگزالات نیز واکنش مشابهی دارد:
Ba۲ + + C۲O۴۲− → BaC۲O۴
این ماده وقتی با هیدروکسید سدیم مخلوط شود، دی هیدروکسید را تشکیل می دهد که به طور متوسط در آب حل می شود.
تشکیل کلرید باریم
این ماده را می توان از هیدروکسید باریم یا کربنات باریم تهیه کرد، ماده دوم به طور طبیعی به عنوان ماده معدنی “Witerite” یافت می شود. این نمک های بازی واکنش می دهند و کلرید باریم هیدراته تولید می کنند.
این ماده در مقیاس صنعتی، از طریق یک فرآیند دو مرحله ای از باریت (سولفات باریم) تهیه می شود:
BaSO۴ + ۴ C → BaS + 4CO
این مرحله اول نیاز به دمای بالا دارد.
BaS + 2 HCl → BaCl۲ + H۲S
به جای HCl می توان از کلر استفاده کرد.
کاربرد های کلرید باریم
اگرچه این ماده ارزان است، اما در آزمایشگاه و صنعت کاربردهای محدودی دارد. در صنعت، از این ماده به طور عمده در تصفیه محلول نمک در گیاهان کلر سوزاننده و همچنین در ساخت نمک های عملیات حرارتی، سخت شدن فولاد استفاده می شود. سمیت آن کاربرد آن را محدود می کند. این ماده عمدتا برای تولید نمک باریم، ابزارهای الکترونیکی و به عنوان نرم کننده آب استفاده می شود.می توان آن را به عنوان عامل دهیدراته کننده و تجزیه و تحلیل استفاده کرد. از این ماده برای ماشینکاری عملیات حرارتی جینگ استفاده می شود.در دستگاه های کالیبراسیون، به منظور ارزیابی و تضمین کیفیت نیز می توان از این ماده استفاده کرد.
این ماده دی هیدرات در تصفیه فاضلاب، تولید تثبیت کننده هایPVC، روان کننده های روغن، کرومات باریم و فلوراید باریم استفاده می شود.معمولاً به عنوان آزمایشی برای یون سولفات استفاده می شود. از این ماده در آتش بازی نیز استفاده می شود تا رنگ سبز روشن به خود بگیرد. با این حال، سمیت آن کاربرد آن را محدود می کند.در صنایع کلر-قلیایی، در ساخت لاستیک از این ماده استفاده می شود.کلرید باریم همچنین به طور گسترده ای در تصفیه روغن، در صنعت کاغذ سازی استفاده می شود.
خصوصیات فیزیکی و شیمیایی کلرید باریم
در شرایط استاندارد، این ماده به صورت یک ماده جامد بلوری سفید وجود دارد (همانطور که در بالا نشان داده شده است). این ماده بی آب در یک ساختار بلوری متبلور می شود. با این حال، شناخته شده است که فرم هیدراته این ماده دارای ساختار بلوری مونو کلینیک است.
در دمای ۲۰ درجه سانتی گراد، حلالیت این ماده در آب تقریباً برابر با ۳۵۸ گرم در لیتر است. با این حال، حلالیت این ترکیب در آب به دما وابسته است. در دمای ۱۰۰ درجه سانتی گراد، حلالیت این ماده در آب برابر با ۵۹۴ گرم در لیتر است. این ترکیب در متانول محلول است.
|
۹۶۳ °C(lit.)
|
Melting point
|
|
۱۵۶۰°C
|
Boiling point
|
|
۳.۸۵۶ g/mL at 25 °C(lit.)
|
Density
|
|
۲-۸°C
|
Storage temp
|
|
H۲O: soluble
|
Solubility
|
| ۳.۹ | Specific Gravity |
|
Beads
|
Form |
|
White
|
Color
|
|
Soluble in water and methanol. Insoluble in acids, ethanol, acetone and ethyl acetate. Slightly soluble in nitric acid and hydrochloric acid.
|
Water Solubility
|
|
Hygroscopic
|
Sensitive
|
 |
Chemical Safety |
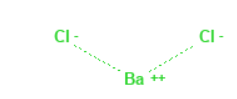 |
Chemical Structure Depiction |
|
۱۰۳۶۱-۳۷-۲
Barium chloride Barium dichloride BaCl۲ Barium chloride (BaCl۲) |
Synonyms |
نکاتی درمورد کلرید باریم
کلرید باریم، همراه با سایر نمک های باریم محلول در آب، بسیار سمی است. سولفات سدیم و سولفات منیزیم مواد خنثی کننده بالقوه ای هستند زیرا آن ها سولفات باریم BaSO۴ را تشکیل می دهند که به دلیل غیر قابل حل بودن نسبتاً غیر سمی است.
کلرید باریم غیر قابل احتراق است. هنگامی که با تری فلوئورید بور تماس پیدا می کند، ممکن است واکنش شدید رخ دهد. بلع یا استنشاق می تواند مسمومیت ایجاد کند، این امر عمدتا از طریق دستگاه تنفسی و دستگاه گوارش به بدن انسان حمله می کند، باعث ریزش و سوزش مری، درد معده، گرفتگی عضلات، حالت تهوع، استفراغ، اسهال، فشار خون بالا می شود. در موارد شدید، می تواند باعث مرگ ناگهانی شود. کلرید باریم همچنین می تواند بر سیستم عصبی مرکزی، سیستم قلبی عروقی و کلیه ها تأثیر منفی بگذارد. یون های باریم می توانند باعث تحریک عضلات شوند، سپس به تدریج منجر به فلج شدن فرد شوند.
منابع :
https://www.solvay.com/en/brands/barium-chloride
https://www.chemicalbook.com/ProductChemicalPropertiesCB8398703_EN.htm
https://pubchem.ncbi.nlm.nih.gov/compound/Barium-chloride
 شرکت اوج آزما پلاست در سال 1392 در ایران تاسیس گردید. هدف اصلی همکاران ما کوشش در جهت بالابردن سطح سلامت در جامعه جهانی است. شرکت اوج آزما پلاست در زمینه واردات و تولیدات تجهیزات و ملزومات آزمایشگاهی و بیمارستانی فعالیت داشته و از ابتدای شروع فعالیت همواره
شرکت اوج آزما پلاست در سال 1392 در ایران تاسیس گردید. هدف اصلی همکاران ما کوشش در جهت بالابردن سطح سلامت در جامعه جهانی است. شرکت اوج آزما پلاست در زمینه واردات و تولیدات تجهیزات و ملزومات آزمایشگاهی و بیمارستانی فعالیت داشته و از ابتدای شروع فعالیت همواره